Ankan là nhóm chất hữu cơ có tính bazơ trong chương trình Hóa học lớp 11. Để hiểu rõ hơn về hợp chất quan trọng này, hãy cùng manta.edu.vn tìm hiểu các lý thuyết trọng tâm bao gồm định nghĩa, tính chất, ứng dụng và điều chế ankan trong bài viết dưới đây.
Định nghĩa của ankan là gì? Dãy đồng đẳng, đồng phân và danh pháp ankan
Ankan là gì? Ankan là hiđrocacbon no mạch hở chỉ có liên kết đơn CC hoặc CH.
Ankan có công thức chung là: CnH2n+2 (n ≥ 1) .
Ankan đơn giản nhất là metan (CH4).
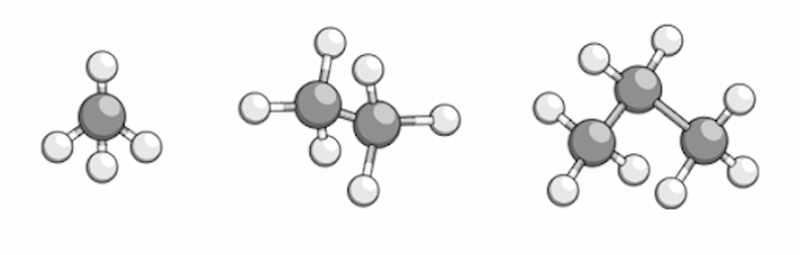
Dãy đồng đẳng ankan
CH4 và các chất có công thức phân tử như C2H6, C3H8, C4H10, C5H12,… được gọi là dãy đồng đẳng ankan có công thức chung CnH2n+2 (n ≥ 1).
-
Chuỗi carbon là chuỗi mở, phân nhánh hoặc không phân nhánh.
-
Trong phân tử ankan, các nguyên tử cacbon phía trong không thẳng hàng (trừ C2H6).
-
Trong phân tử chỉ có liên kết đơn được tạo thành từ 4 obitan lai hoá sp3 trong nguyên tử cacbon định hướng tứ diện đều. Do đó, chuỗi carbon bị uốn cong và các nguyên tử carbon có thể quay khá tự do xung quanh các liên kết đơn.
đồng phân
Từ C4H10 trở đi, mỗi công thức phân tử sẽ tương ứng với công thức cấu tạo của mạch cacbon không phân nhánh và mạch cacbon phân nhánh của các đồng phân mạch cacbon.
Ví dụ công thức phân tử C2H5 sẽ tương ứng với số đồng phân cấu tạo như sau:
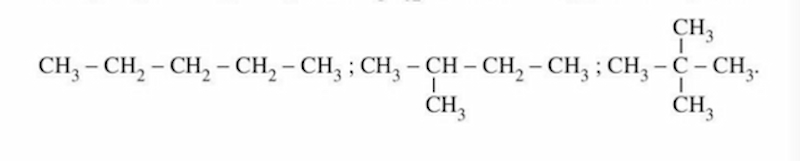
Danh pháp ankan
Một số ankan mạch cacbon không phân nhánh với các danh pháp khác nhau được trình bày trong bảng dưới đây:
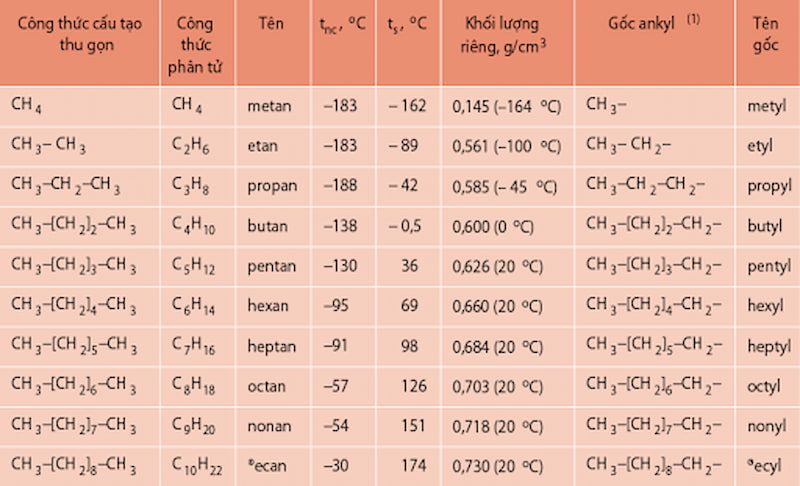
-
Tên các ankan mạch thẳng
Tên ankan mạch thẳng = Tên mạch cacbon + an
Ví dụ:
CH4: Metan
C2H6: Etan
C3H8: Propan
C4H10: Butan
-
Tên các ankan mạch nhánh
Tên nhánh của ankan = Vị trí nhánh – tên nhánh + tên mạch chính + an. Phía trong:
-
Số chuỗi cacbon là chuỗi dài nhất và nhiều nhánh nhất.
-
Các nguyên tử cacbon của chuỗi chính được đánh số bắt đầu từ phía gần nhánh nhất.
-
Gọi tên mạch nhánh (nhóm ankyl) theo thứ tự bảng chữ cái kèm theo số vị trí của nó, sau đó là ankan tương ứng với mạch chính (chi tiết ở bảng trên).
-
Gốc hiđrocacbon là phần còn lại của phân tử hiđrocacbon sau khi đã loại bỏ một số nguyên tử hiđro, nhưng vẫn tồn tại trong phân tử ở trạng thái liên kết và không mang điện tử tự do như các gốc tự do.
-
Công thức chung của nhóm ankyl là: CnH(2n+1)
-
Bậc của nguyên tử cacbon trong phân tử ankan bằng số nguyên tử cacbon liên kết trực tiếp với nó.
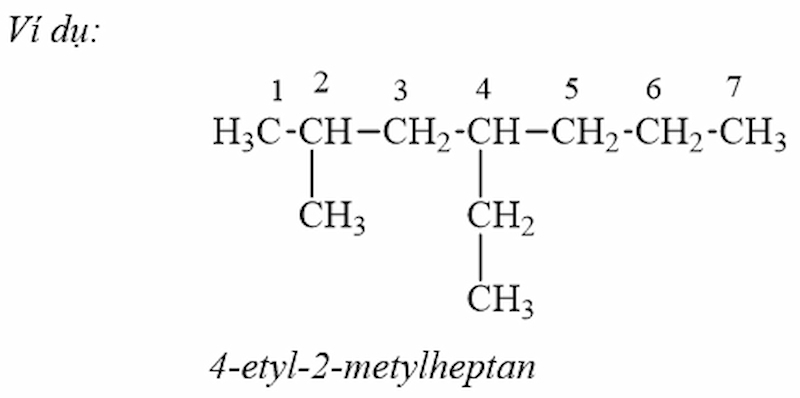
Trong trường hợp nguyên tử C bậc 2 chỉ có một nhánh CH3 thì ta thêm tiền tố iso vào cuối.
Trường hợp 2 nhánh CH3 ở nguyên tử C 2 thì ta thêm tiền tố neo.
Tính chất vật lý của ankan
Dưới đây là các tính chất vật lý của ankan mà bạn cần biết:
-
Ở điều kiện thường, 4 ankan đầu tiên trong dãy đồng đẳng (CH4 đến C4H10) tồn tại ở thể khí. Các ankan tiếp theo là chất lỏng và từ C18H38 trở đi là chất rắn.
-
Theo chiều tăng phân tử khối thì nhiệt độ nóng chảy, nhiệt độ sôi và khối lượng riêng của ankan tăng dần.
-
Ankan nhẹ hơn nước, đa số ankan không tan trong nước mà chỉ tan trong dung môi hữu cơ.
-
Ankan là dung môi không phân cực, tan được trong các chất không phân cực như benzen, dầu mỡ…
Tính chất hóa học của ankan
Ở nhiệt độ phòng, ankan không phản ứng với dung dịch axit, dung dịch kiềm và chất oxy hóa. Nhưng khi đun nóng hoặc chiếu sáng, ankan dễ dàng tham gia các phản ứng thế, phản ứng tách hiđro, phản ứng cháy. Hãy cùng tìm hiểu tính chất hóa học của ankan qua 3 phản ứng tiêu biểu nhất.

Phản ứng thế của halogen
Clo có thể thay thế lần lượt từng nguyên tử H trong phân tử metan :
- CH4 + Cl2 → CH3Cl (clometan – metyl clorua) + HCl (DR: Ánh sáng)
- CH3Cl + Cl2 → CH2Cl2 (điclometan-metylen clorua) + HCl (DR: Ánh sáng)
- CH2Cl2 + Cl2 → CHCl3 (triclorometan – clorofom) + HCl (DR: Ánh sáng)
- CHCl3+Cl2 → CCl4 (tetrachloromethane- carbon tetrachloride) + HCl (DR: Ánh sáng)
Các đồng phân của metan cũng tham gia phản ứng thế giống metan là:
- CH3-CH2-CH3 + Br2 → CH3-CHBr-CH3 + HBr (sản phẩm chính)
- CH3-CH2-CH3 + Br2 → CH3-CH2-CH2-Br + HBr (sản phẩm phụ)
Đối với các ankan có chuỗi cacbon từ 3 C trở lên, clo và brom sẽ ưu tiên thế H ở các cacbon cao hơn tạo thành sản phẩm chính.
Vì ankan phản ứng mãnh liệt với flo nên chúng sẽ phân hủy thành C và HF: CnH2n+2 + (n+1)F2 → nC + (2n+2)HF
Các ankan không phản ứng theo cách đó với iốt.
Khả năng phản ứng của dãy halogen với ankan giảm dần theo thứ tự: F2 > Cl2 > Br2 > I2.
Nhận xét :
-
Nguyên tử hydro liên kết với nguyên tử carbon cao hơn dễ bị ảnh hưởng hơn so với nguyên tử hydro liên kết với nguyên tử carbon thấp hơn.
-
Sản phẩm thế gọi là dẫn xuất halogen của hiđrocacbon.
phản ứng tách
Dưới tác dụng của nhiệt và xúc tác thích hợp, các ankan có khối lượng phân tử nhỏ sẽ bị tách hiđro thành hiđrocacbon không no tương ứng.
Ví dụ: CH3 – CH3 → CH2=CH2 + H2 (500 độ C, xúc tác)
Phương trình tổng quát: CnH(2n+2) → CnH2n + H2 (nhiệt độ, Fe)
Ở nhiệt độ cao và xúc tác thích hợp, ngoài phản ứng dehiđro hóa, ankan còn có thể bị phân cắt mạch cacbon để tạo thành phân tử nhỏ hơn.
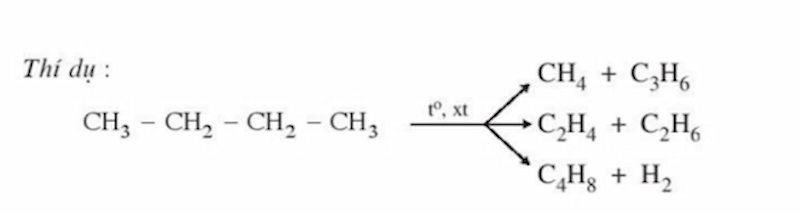
Ghi chú:
-
Ankan có 2 nguyên tử C trở lên tham gia phản ứng tách H2.
-
Trong phản ứng này 2 nguyên tử H với 2 nguyên tử C ở cạnh nhau sẽ cùng nhau tách ra. Nên ưu tiên tách nguyên tử H ở nguyên tử C bậc cao hơn. C4H10 → CH3 – CH=CH – CH3 + H2 (Fe nhiệt độ)
phản ứng oxy hóa
Khi đốt cháy các ankan đều cháy và toả nhiều nhiệt theo công thức chung là:
CnH2n+2 + (3n+1/2)O2 → nCO2 + (n+1)H2O
Nếu thiếu oxi thì phản ứng cháy của ankan xảy ra không hoàn toàn: Sản phẩm cháy còn có C, CO,.. ngoài CO2 và nước.
Bình luận:
-
Đốt cháy ankan thu được nCO2 < nH2O
-
Đốt cháy hiđrocacbon ta thu được nCO2 < nH2O. Hiđrocacbon bị đốt cháy là ankan (CnH2n+2).
Điều chế ankan trong phòng thí nghiệm và trong công nghiệp
Ankan được tạo ra ở đâu? Hãy cùng manta.edu.vn tìm hiểu cách điều chế hợp chất này trên 2 môi trường: Phòng thí nghiệm và công nghiệp.
Điều chế ankan trong phòng thí nghiệm
Trong phòng thí nghiệm, metan được điều chế bằng cách đun nóng natri axetat khan với hỗn hợp vôi và xút theo phương trình:
CH3COONa + NaOH → CH4↑ + Na2CO3 (Quy định: CaO, nhiệt độ)
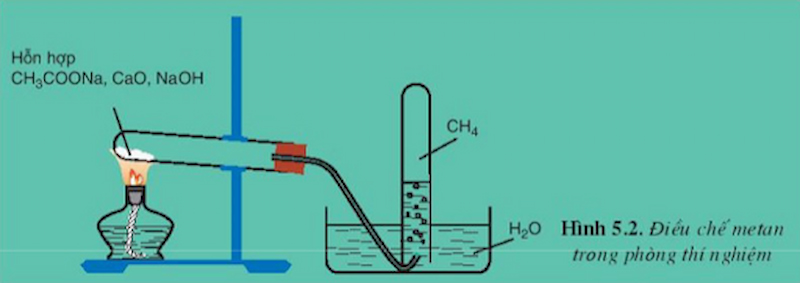
Điều chế ankan trong công nghiệp
Một lượng lớn ankan (CH4, C2H6, C3H8, C4H10…) được tìm thấy trong dầu mỏ, khí dầu mỏ, khí tự nhiên, v.v… Bằng phương pháp chưng cất phân đoạn, người ta thu được các ankan công nghiệp ở dạng phân đoạn. chưng cất khác nhau .
- C + 2H2 → CH4 (Ni, 500 độ C)
- CO + 3H2 → CH4 + H2O (nhiệt độ, xúc tác)
Ứng dụng của các ankan phổ biến
Với những tính chất vật lý và hóa học trên, ankan mang đến những ứng dụng đa dạng và khác nhau trong đời sống thực tế. Đặc trưng:
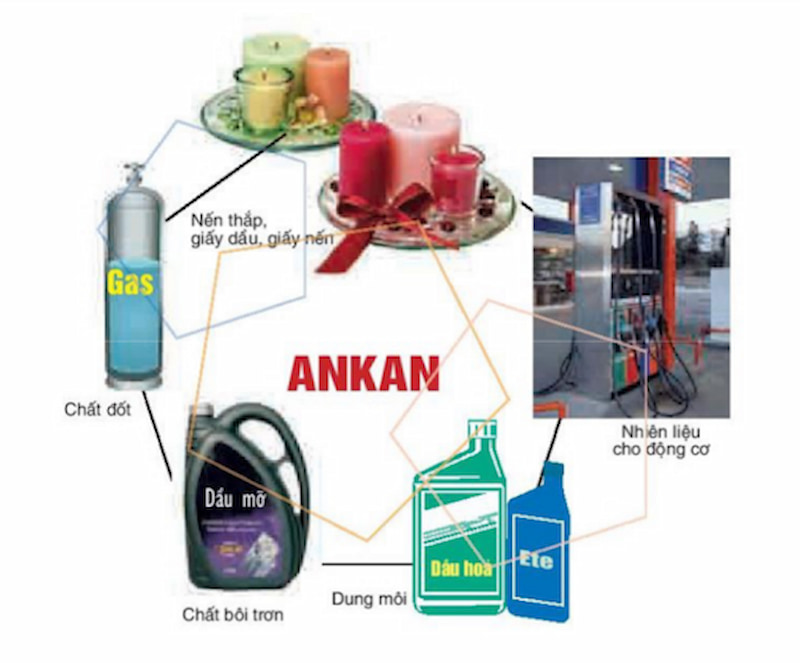
-
Nhiên liệu trong hàn cắt kim loại.
-
Chất bôi trơn và dung môi.
-
Dùng để tổng hợp nhiều chất hữu cơ khác như: CH3Cl, CH2Cl2, CCl4, CF2Cl2,…
-
Đặc biệt, CH4 có thể ứng dụng để điều chế nhiều chất khác nhau như: hỗn hợp CO + H2, amoniac, C2H2, ancol metylic, anđehit fomic,…
So sánh ankan, anken, ankin
Từ cấu tạo và tính chất ta có bảng so sánh ankan, anken và ankin như sau:
| Ankan | Anken | Ankin | |
| Thành phần nguyên tố | Gồm 2 nguyên tố C và H | ||
| Công thức phân tử | CnH(2n+2) (n>= 1) | CnH2n (n>=2) | CnH(2n-2) (n>=2) |
| Liên kết hóa học | Gồm chỉ liên kết đơn | Gồm 1 liên kết đôi và các liên kết đơn | Gồm 1 liên kết 3 và các liên kết đơn |
| Tính chất hóa học | Đều có phản ứng cháy | ||
| Phản ứng thế | Phản ứng cộng
Phản ứng oxy hóa (không hoàn toàn) Phản ứng trùng hợp |
Phản ứng cộng
Phản ứng oxy hóa (không hoàn toàn) Dime hóa, trime hóa |
|
Bài tập ankan SGK Hóa 11 có lời giải chi tiết
Để có được những kiến thức đầy đủ nhất về ankan , hãy cùng manta.edu.vn vận dụng lý thuyết đã học vào thực hành một số bài tập cơ bản trong SGK Hóa học 11 dưới đây.

Bài 1 (trang 115 SGK Hóa 11)
Hiđrocacbon no, ankan, xicloankan là gì?
Câu trả lời gợi ý:
Hiđrocacbon no là hiđrocacbon trong phân tử chỉ có liên kết đơn. Hydrocacbon no được chia thành hai loại:
-
Ankan (hay parafin) là những hiđrocacbon no không có mạch vòng.
-
Xicloankan là hiđrocacbon no mạch vòng.
Hiđrocacbon no là nguồn nhiên liệu chính và là nguồn nguyên liệu quan trọng của công nghiệp hoá chất.
Bài 2 (trang 115 SGK Hóa 11)
Viết công thức phân tử của các hiđrocacbon tương ứng với các gốc ankyl sau: –CH3 ; -C3H7; -C6H13
Câu trả lời gợi ý:
|
Gốc ankan |
CTPT của hiđrocacbon tương ứng |
|
-CH3 |
CH4 |
|
-C3H7 |
C3H8 |
|
-C6H13 |
C6H14 |
Bài 4 (trang 116 SGK Hóa 11)
Hiđrocacbon no được dùng làm nhiên liệu vì lý do nào sau đây?
A. Hiđrocacbon no có phản ứng thế.
B. Hiđrocacbon no có nhiều trong tự nhiên.
C. Hiđrocacbon no là chất nhẹ hơn nước.
D. Hiđrocacbon no tỏa nhiều nhiệt, có nhiều trong tự nhiên
Trả lời : Đáp án D.
Bài 5 (trang 116 SGK Hóa 11)
Vui lòng giải thích:
a) Tại sao không được để các thùng chứa xăng, dầu (kể cả ankan) gần ngọn lửa, trong khi người ta có thể nấu chảy nhựa đường để làm đường giao thông.
b) Không dùng nước để dập tắt đám cháy xăng, dầu mà phải dùng bình cát hoặc bình khí cacbonic.
Câu trả lời gợi ý:
a) Không để các dụng cụ chứa xăng, dầu gần lửa vì: Xăng chứa ankan mạch ngắn, dễ bay hơi, rất dễ cháy. Nhưng người ta có thể nấu chảy nhựa đường để làm đường vì nhựa đường chứa ankan có mạch cacbon rất lớn, khó bay hơi và rất khó bắt cháy.
b) Không dùng nước để dập các đám cháy xăng dầu mà phải dùng cát hoặc bình khí cacbonic vì: Xăng, dầu nhẹ hơn nước; Khi sử dụng nước, xăng, dầu sẽ nổi lên mặt nước khiến ngọn lửa bùng cháy lớn hơn. Khi dùng cát hoặc thùng chứa khí cacbonic sẽ ngăn không cho xăng, dầu tiếp xúc với oxi nên đám cháy được dập tắt.
Bài 7 (trang 116 SGK Hóa 11)
Khi đốt cháy hoàn toàn 3,6g ankan X thu được 5,6 lít CO2 (dktc). Công thức phân tử của X là:
A. C3H8 ;
B. C5H10
C. C5H12 ;
D. C4H10
Câu trả lời gợi ý:
Gọi công thức phân tử của ankan là: CnH2n+2
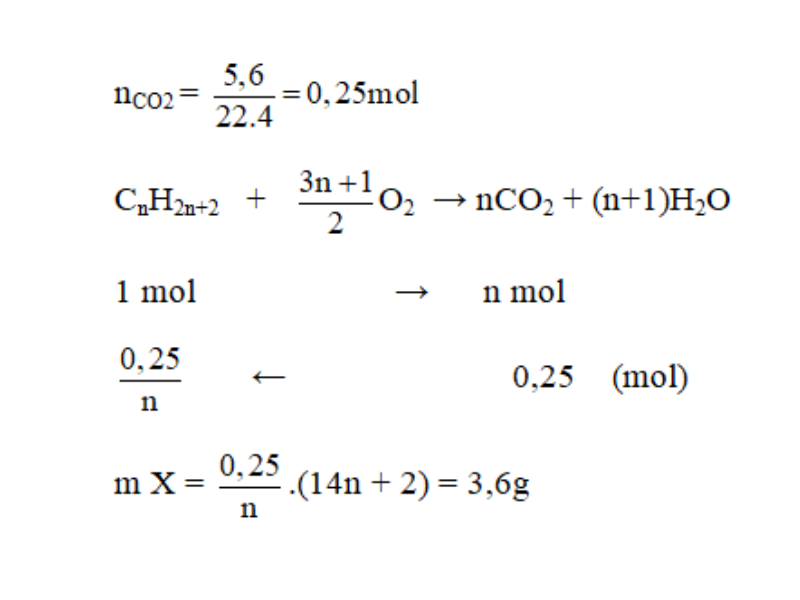
⇒ n = 5 ankan là C5H12
Vậy đáp án đúng là C.
Bài tập vận dụng tính chất hóa học của ankan dành cho học sinh tự luyện
Ngoài các bài tập trong SGK Hóa học 10, dưới đây là một số bài tập liên quan để các bạn cùng luyện tập:
Câu 1: Hợp chất hữu cơ X có tên gọi là: 2 – Clo – 3 – metylpentan. Công thức cấu tạo của X là:
A. CH3CH2CH(Cl)CH(CH3)2
B. CH3CH(Cl)CH(CH3)CH2CH3
C. CH3CH2CH(CH3)CH2CH2Cl
D. CH3CH(Cl)CH2CH(CH3)CH3
Câu 2: Có bao nhiêu đồng phân cấu tạo có công thức phân tử C5H12?
A. 3 đồng phân
B. 4 đồng phân
C. 5 đồng phân
D. 6 đồng phân
Câu 3: Có bao nhiêu đồng phân cấu tạo có công thức phân tử C6H14?
A. 3 đồng phân
B. 4 đồng phân
C. 5 đồng phân
D. 6 đồng phân
Câu 4: Có bao nhiêu đồng phân cấu tạo có công thức phân tử C4H9Cl?
A. 3 đồng phân
B. 4 đồng phân
C. 5 đồng phân
D. 6 đồng phân
Câu 5: Có bao nhiêu đồng phân cấu tạo có công thức phân tử C5H11Cl?
A. 6 đồng phân
B. 7 đồng phân
C. 5 đồng phân
D. 8 đồng phân
Câu 6: Phần trăm khối lượng cacbon trong phân tử của ankan Y là 83,33%. Công thức phân tử của Y là:
A. C2H6
B. C3H8
C. C4H10
D. C5H12
Câu 7: Công thức đơn giản nhất của hiđrocacbon M là CnH2n+1. M thuộc dãy đồng đẳng nào?
A. ankan
B. không đủ dữ liệu để xác định
C. ankan hoặc xicloankan
D. xicloankan
Câu 8: Cho ankan có công thức: (CH3)2CHCH2C(CH3)3. Tên của ankan là
A. 2,2,4-trimetylpentan.
B. 2,4-trimetylpetan.
C. 2,4,4-trimetylpentan.
D. 2-đimetyl-4-metylpentan.
Câu 9: Cho iso-pentan tác dụng với Cl2 theo tỉ lệ mol 1:1, số sản phẩm đơn chức tối đa thu được là
A. 2
B.3.
C.5.
D.4.
Câu 10: Iso-hexan phản ứng được với bao nhiêu dẫn xuất monoclo (có chiếu sáng)?
A. 3
B 4
C. 5
mất 6
Câu 11: Khi cho 2-metylbutan tác dụng với Cl2 theo tỉ lệ mol 1:1 thu được sản phẩm chính là
A. 1-clo-2-metylbutan.
B. 2-clo-2-metylbutan.
C. 2-clo-3-metylbutan.
D. 1-clo-3-metylbutan.
Câu 12: Khi clo hóa C5H12 theo tỉ lệ số mol 1:1 thu được 3 sản phẩm thế monoclo. Danh pháp IUPAC của ankan đó là
A. 2,2-đimetylpropan.
B. 2-metylbutan.
C. pentan.
D. 2-đimetylpropan.
Câu 13: Khi clo hóa metan thu được sản phẩm thế chứa 89,12% clo theo khối lượng. Công thức của sản phẩm là
A. CH3Cl.
B. CH2Cl2.
C. CHCl3.
D. CCl4.
Câu 14: Cho 4 chất: metan, etan, propan và n-butan. Số chất có thể tạo thành một sản phẩm thế monoclo duy nhất là
MỘT.1.
B.2.
C.3.
D.4.
Câu 15: Khi clo hóa một ankan có công thức phân tử C6H14 chỉ thu được 2 sản phẩm thế đơn chức. Danh pháp IUPAC của ankan đó là
A. 2,2-đimetylbutan.
B. 2-metylpentan.
C. n-hexan.
D. 2,3-đimetylbutan.
Câu 16: Khi clo hóa hỗn hợp 2 ankan chỉ thu được 3 sản phẩm thế monoclo. Tên của hai ankan là:
A. etan và propan.
B. propan và iso-butan.
C. iso-butan và n-pentan.
D. neo-pentan và etan.
Câu 17: Khi brom hóa một ankan chỉ thu được một dẫn xuất monobrom duy nhất có tỉ khối hơi đối với hiđro là 75,5. Tên của ankan đó là
A. 3,3-đimetylhexan.
C. isopentan.
B. 2,2-đimetylpropan.
D. 2,2,3-trimetylpentan
Câu 18: Khi cho ankan X (trong phân tử có phần trăm khối lượng cacbon bằng 83,72%) phản ứng với clo theo tỉ lệ mol 1:1 (trong điều kiện chiếu sáng) chỉ thu được 2 dẫn xuất đơn chức của đồng phân. phân của nhau. X tên là
A. 3-metylpentan.
B. 2,3-đimetylbutan.
C. 2-metylpropan.
D. butan.
Câu 19: Hiđrocacbon X mạch hở trong phân tử chỉ chứa liên kết σ và có hai cacbon bậc ba trong phân tử. Đốt cháy hoàn toàn 1 thể tích X sinh ra 6 thể tích CO2 (ở cùng điều kiện nhiệt độ và áp suất). Khi cho X phản ứng với Cl2 (theo tỉ lệ mol 1:1) thì số dẫn xuất monoclo tối đa tạo ra là
MỘT.3.
B 4.
C.2.
D.5.
Câu 20: Khi tiến hành phản ứng thế giữa ankan X bằng khí clo có chiếu sáng, thu được hỗn hợp Y chỉ chứa hai sản phẩm. Tỉ khối hơi của Y đối với hiđro là 35,75. Tên của X là:
A. 2,2-đimetylpropan.
B. 2-metylbutan.
C. pentan.
D. 2-đimetylpropan.
Câu 21: Khi cho ankan X (trong phân tử có phần trăm khối lượng cacbon bằng 83,72%) phản ứng với khí Cl2 theo tỉ lệ số mol 1:1 (trong điều kiện chiếu sáng) chỉ thu được hai dẫn xuất monoclo đồng thời. phân của nhau. Tên của X là gì?
Câu 22: Cracking 22,4 lít khí C4H10 (ở dtc) thu được hỗn hợp A gồm CH4, C2H6, C2H4, C3H6, C4H8, H2 và C4H10. Đốt cháy hoàn toàn A thu được x gam CO2 và y gam H2O. Tính giá trị của x và y.
Câu 23: Khi crackinh hoàn toàn một ankan X thu được hỗn hợp Y (các thể tích khí đo ở cùng điều kiện nhiệt độ và áp suất); Tỉ khối của Y so với H2 là 29. Công thức phân tử của X là?
Câu 24: Cracking 8,8 gam propan thu được hỗn hợp A gồm H2, CH4, C2H4, C3H6 và một phần propan chưa bị crackinh. Giả thiết hiệu suất phản ứng là 90%. Khối lượng phân tử trung bình của A là?
Câu 25: Cracking 40 lít n–butan thu được 56 lít hỗn hợp A gồm H2, CH4, C2H4, C2H6, C3H6, C4H8 và một phần n-butan. Các thể tích khí đo ở cùng điều kiện về nhiệt độ và áp suất. Giả sử chỉ có các phản ứng tạo ra các sản phẩm trên. Hiệu suất % của phản ứng tạo thành hỗn hợp A là bao nhiêu?
Như vậy, bài viết trên đã giúp bạn đọc có thêm những kiến thức cơ bản về ankan bao gồm: Ankan là gì, tính chất vật lý, hóa học, ứng dụng và điều chế. manta.edu.vn hi vọng các em vận dụng tốt những kiến thức này vào các bài tập thực hành môn Hóa học cũng như trong thực tế cuộc sống. Đừng quên truy cập website manta.edu.vn mỗi ngày để cập nhật những thông tin thú vị khác về Hóa học nhé!



