Phân bón hóa học là chất xúc tác không thể thiếu trong sản xuất nông nghiệp, với vai trò cung cấp các chất dinh dưỡng cần thiết cho cây trồng, tạo nên một vụ mùa bội thu. Trong bài viết này, Manta.edu.vn sẽ cùng các em tìm hiểu kỹ hơn về các loại phân bón này và hướng dẫn giải chi tiết các bài tập trong SGK.
Phân bón hóa học là gì?
Phân bón hóa học (hay còn gọi là phân bón vô cơ) là loại phân hóa học có chứa nhiều nguyên tố dinh dưỡng. Chúng được áp dụng cho cây trồng để cải thiện năng suất cây trồng. Thông thường, đất trở nên nghèo chất dinh dưỡng khi cây phát triển. Do đó, cây trồng cần hấp thụ các chất dinh dưỡng bổ sung từ đất.

Phân bón hóa học phổ biến nhất
Phân bón hóa học thường chứa các chất dinh dưỡng cần thiết cho cây trồng như: P, Ca, N, K, Zn, Mg, Cu,… Căn cứ vào thành phần các nguyên tố dinh dưỡng khác nhau, người ta chia phân bón hóa học thành các loại chính, đó là:

-
phân đạm
-
phân lân
-
phân kali
-
Phân bón hỗn hợp và hợp chất
-
phân vi lượng
Phân bón hóa học – Phân đạm
Phân đạm là loại phân hóa học được sử dụng rộng rãi và phổ biến nhất hiện nay. Chúng có vai trò kích thích sinh trưởng, giúp cây trồng phát triển nhanh hơn, cho ra các sản phẩm như hạt, củ hay quả chất lượng hơn. Phân đạm sẽ cung cấp đạm cho cây trồng dưới dạng ion amoni NH4+ và nitrat NO3-. Tỷ lệ Nitơ trong phân sẽ quyết định mức độ dinh dưỡng của loại phân hóa học này. Dưới đây là các loại phân đạm phổ biến nhất.

phân đạm amoni
Phân đạm amoni là sản phẩm của các muối amoni điển hình như NH4Cl, (NH4)2SO4, NH4NO3…
Tự nhiên:
-
Dễ tan trong nước giúp cây trồng dễ hấp thụ, đồng thời cũng dễ bị nước rửa trôi.
-
Thành phần của nó có chứa gốc NH4+ nên khi gặp nước dễ làm tăng độ chua của đất. Vì vậy, phân đạm amoni không thích hợp sử dụng cho đất chua.
Để điều chế phân đạm amoni, người ta cho amoniac phản ứng với axit tương ứng.
Ví dụ: 2NH3 + H2SO4 → (NH4)2SO4
phân đạm
Phân đạm nitrat là sản phẩm của các muối nitrat như NaNO3, Ca(NO3)2… Loại phân bón này được điều chế bằng phản ứng giữa axit nitric và muối cacbonat.
Tính chất: Nito nitrat dễ tan trong nước, rất dễ chảy. Vì vậy, khi bón vào đất đạm nitrat có tác dụng nhanh đối với cây trồng nhưng cũng dễ bị rửa trôi khi gặp nước mưa.
Ví dụ: CaCO3 + 2HNO3 → Ca(NO3)2 + CO2 + H2O
phân urê
Phân Urê có công thức hóa học là (NH2)2CO chứa tới 46% N, là loại phân đạm tốt nhất hiện nay.
Ure được điều chế bằng cách cho amoniac phản ứng với CO2 ở nhiệt độ 180 – 200 độ C, áp suất khoảng 200 atm.
Ví dụ: CO2 + 2NH3 → (NH2)2CO + H2O (nhiệt độ, p)
Tự nhiên:
-
Urê là chất rắn màu trắng, tan rất tốt trong nước và dễ bị mất nước như các loại phân đạm khác.
-
Trong đất, urê bị phân hủy dưới tác dụng của vi sinh vật. Sản phẩm sinh ra là amoniac hoặc chuyển dần sang muối cacbonat khi gặp nước.
(NH2)2CO + 2H2O → (NH4)2CO3
Từ những thông tin về các loại phân hóa học trên ta có bảng tổng hợp và so sánh các loại phân đạm như sau:
| phân đạm | Nguyên liệu | Ion thực vật hấp thụ | Tự nhiên | điều chế |
| amoniac | Muối amoni NH4Cl, (NH4)2SO4, NH4NO3 | NH4+, NO3– | Hòa tan tốt trong nước, dễ dàng rửa sạch. | Cho amoniac phản ứng với axit tương ứng. |
| nitrat | Muối nitrat NaNO3, Ca(NO3)2,… | SỐ 3- | Hòa tan tốt trong nước, dễ dàng rửa sạch. | Muối cacbonat MCO3 phản ứng với HNO3. |
| urê | (NH2)2CO | NH4+ |
Chất rắn màu trắng, tan tốt trong nước. Có hàm lượng N cao nhất. |
Cho CO2 phản ứng với NH3 ở 180-2000C dưới áp suất 200 atm. |
Phân bón hóa học 11 – Phân lân
Bên cạnh phân đạm, phân lân cũng là một dạng phân hóa học quan trọng. Chúng cung cấp lân cho cây trồng trong suốt thời kỳ sinh trưởng, thúc đẩy các quá trình sinh hóa, trao đổi chất, trao đổi năng lượng của cây trồng. Giá trị dinh dưỡng của phân lân phụ thuộc vào phần trăm khối lượng của P2O5 có trong thành phần.

Nguyên liệu để sản xuất phân lân là quặng apatit và photphoric. Hai loại phân lân được sử dụng phổ biến nhất hiện nay, đó là: Supe lân và Phân lân nung chảy.
superphotphat
Supe lân được chia thành 2 loại:
supe lân đơn
-
Gồm 2 muối Ca(H2PO4)2 (dễ tan) và CaSO4 (không tan, làm đất rắn chắc).
-
Chứa 14 – 20% P2O5. Chúng được điều chế bằng cách cho bột quặng photphorit hoặc apatit phản ứng với axit sunfuric đậm đặc:
Ca3(PO4)2 + 2H2SO4 (đậm đặc) → Ca(H2PO4)2 + 2CaSO4 (kết tủa)
superphotphat kép
-
Chứa hàm lượng P2O5 từ 40-50%, do chỉ chứa Ca(H2PO4)2.
-
Loại phân hóa học này được điều chế qua 2 giai đoạn:
Giai đoạn 1 : Điều chế axit photphoric
Ca3(PO4)2 + 3H2SO4 → 2H3PO4 + 3CaSO4 (kết tủa)
Giai đoạn 2 : Cho axit photphoric phản ứng với apatit hoặc photphorit
Ca3(PO4)2 + 4H3PO4 → 3Ca(H2PO4)2
Phân lân nung chảy
Phân lân nung chảy có thành phần chính là phốt phát và các silicat của canxi và magie. Chúng chứa 12 – 14% P2O5, chỉ thích hợp với đất chua vì loại muối này khó tan trong nước.
Phân lân nung chảy được điều chế như sau: Nung hỗn hợp bột quặng apatit, đá hàu và than cốc ở nhiệt độ trên 1000 độ C, trong lò đứng. Sản phẩm nóng chảy sau đó được làm nguội nhanh bằng nước, sấy khô và tán thành bột.
Từ những thông tin về các loại phân hóa học trên, ta có bảng tổng hợp và so sánh các loại phân lân như sau:
| Loại phân chuồng | Nguyên liệu | Ion đồng hóa thực vật | phương pháp điều chế | Nội dung |
| supe lân đơn | Ca(H2PO4)2 và CaSO4 | H2PO4– | 14-20% | |
| superphotphat kép | Ca(H2PO4)2 | H2PO4– |
Giai đoạn 1: Điều chế axit photphoric Ca3(PO4)2 + 3H2SO4 → 2H3PO4 + 3CaSO4 Giai đoạn 2: Cho axit photphoric phản ứng với apatit hoặc photphorit Ca3(PO4)2 + 4H3PO4 → 3Ca(H2PO4)2 |
40-50% |
| Đổ tan chảy | Hỗn hợp phốt phát và silicat của canxi và magiê. | Nung hỗn hợp gồm bột quặng apatit, đá xà phòng (thành phần chính là magie silicat) và than cốc trong lò đứng có nhiệt độ trên 1000 độ C. | 12-14% |
phân bón hóa học kali
Phân kali là loại phân bón hóa học cung cấp cho cây trồng nguyên tố kali ở dạng ion K+. Trong nông nghiệp, phân bón hóa học kali thường được sử dụng cùng với các loại phân bón khác giúp thúc đẩy quá trình tạo chất xơ, đường, dầu, tăng khả năng chịu hạn, chịu rét, chống chịu sâu bệnh. bệnh cây trồng. Độ dinh dưỡng của phân kali được xác định dựa trên phần trăm khối lượng của K2O trong bảng thành phần.

Muối KCl và K2SO4 là nguyên liệu được sử dụng nhiều nhất trong sản xuất phân kali. Tro thực vật có chứa K2CO3 trong thành phần của nó cũng được coi là một loại phân kali.
Phân bón hỗn hợp và hợp chất
Phân hỗn hợp và phân hỗn hợp là phân hóa học có chứa một số chất dinh dưỡng cơ bản cùng một lúc.

-
Phân hỗn hợp (hay còn gọi là phân NPK): Thành phần của chúng bao gồm: Đạm, Lân, Kali. Ví dụ nitrophotka là hỗn hợp của KNO3 và (NH4)2HPO4. Tùy theo loại cây trồng và loại đất mà bà con chọn loại phân bón có tỷ lệ N:P:K thích hợp.
-
Phân phức hợp: Là loại phân bón có chứa hỗn hợp các chất được tạo ra đồng thời do tương tác hóa học giữa các chất. Ví dụ, phản ứng của amoniac với axit photphoric tạo ra một amophotphat phức tạp chứa hỗn hợp các muối NH4H2PO4 và (NH4)2HPO4.
phân vi lượng
Cũng giống như “vitamin cho cây trồng”, phân vi lượng là một loại phân bón hóa học cung cấp cho cây trồng các nguyên tố dinh dưỡng như kẽm, bo, đồng, mangan, molypden… giúp tăng trưởng và trao đổi chất. chất lượng và tăng hiệu quả quang hợp của cây trồng.

Phân vi lượng thường được bón vào đất với lượng nhỏ, kết hợp với phân hữu cơ hoặc vô cơ. Phân vi lượng chỉ có tác dụng với từng loại cây trồng và từng loại đất, nếu sử dụng với liều lượng không phù hợp sẽ gây hại cho cây trồng.
Bài tập phân bón hóa học SGK 11 có lời giải chi tiết
Hãy cùng Manta.edu.vn vận dụng những kiến thức chi tiết về phân bón hóa học nêu trên vào làm bài tập giải bài tập phân bón hóa học SGK 11 dưới đây.

Bài 1 (SGK Hóa học 11, trang 58)
Cho các mẫu phân đạm sau: Amoni sunfat, amoni clorua, natri nitrat. Dùng thuốc thử thích hợp để phân biệt chúng. Viết phương trình hóa học các phản ứng đã dùng?
Câu trả lời gợi ý:
Ta hòa tan một ít mẫu phân đạm vào nước ta được 3 dung dịch muối: (NH4)2SO4, NH4Cl, NaNO3. Thêm từ từ dung dịch Ba(OH)2 vào từng dung dịch:
-
Nếu thấy dung dịch nào có mùi khí và kết tủa trắng là (NH4)2SO4
(NH4)2SO4 + Ba(OH)2 → BaSO4 + 2NH3 ↑+ 2H2O
-
Nếu thấy dung dịch nào có mùi khí thì đó là NH4Cl.
2NH4Cl + Ba(OH)2 → BaCl2 + 2NH3 + 2H2O
-
Dung dịch không có hiện tượng gì là NaNO3
Bài 2 (SGK Hóa học 11, trang 58)
Từ không khí, than, nước và các chất xúc tác cần thiết, hãy lập sơ đồ điều chế phân đạm NH4NO3.
Câu trả lời gợi ý:
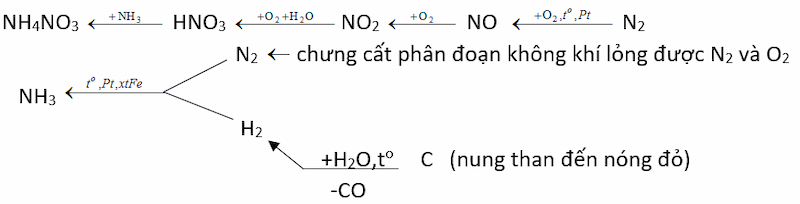
Bài 3 (trang 58 SGK Hóa 11)
Một loại quặng photphat chứa 35% Ca3(PO4)2. Tính phần trăm khối lượng P2O5 có trong quặng trên.
Câu trả lời gợi ý:
Trong 1000g quặng có: 1000. 35% = 350g Ca3(PO4)2
Bảo toàn nguyên tố P trong 1 mol Ca3(PO4)2 bằng 1mol P2O5 tức là trong 310g Ca3(PO4)2 có 142g P2O5 tương ứng.
⇒350g Ca3(PO4)2 có lượng P2O5 là:
m(P2O5) = 350 x 142/310 = 160,3g
% P2O5 trong quặng = 160,3 x 100%/1000 = 16,03%
Bài 4 (SGK Hóa học 11, trang 58)
Để sản xuất một lượng phân amophotphat đã dùng hết 6000.10^3 mol H3PO4.
a) Tính thể tích khí amoniac cần dùng, biết rằng loại lưỡng tính này có tỉ lệ mol nNH4H2PO4 : n(NH4)2HPO4 = 1 : 1.
b) Tính khối lượng amophotphat thu được.
Câu trả lời gợi ý:
Phương trình phản ứng:
H3PO4 + NH3 → NH4H2PO4
H3PO4 + 2NH3 → (NH4)2HPO4
⇒ Phương trình phản ứng tổng hợp:
2H3PO4 + 3NH3 → NH4H2PO4 + (NH4)2HPO4
một. Từ phương trình phản ứng ta có:
∑mol NH3 cần dùng = 1,5 mol H3PO4 = 1,5 x 6 x 10^3 = 9000 (mol)
⇒ VNH3 (chiếc) = 9000 x 22,4 = 201600 (lít)
b. Từ phương trình phản ứng ta có:
nNH4H2PO4 = n(NH4)2HPO4 = 0,5.nH3PO4 = 0,5 x 6 x 10^3 = 3000 (mol)
Khối lượng amophotphat thu được:
mNH4H2PO4 + m(NH4)2HPO4 = 3000 x (115+132) = 741000(g) =741(kg).
Cây muốn phát triển tốt, ngoài điều kiện về ánh sáng, nước cần được cung cấp đầy đủ chất dinh dưỡng thông qua phân bón hóa học. Hi vọng bài viết trên đã giúp bạn đọc có thêm nhiều kiến thức thú vị xung quanh phân bón hóa học và ứng dụng hiệu quả những thông tin này trong cuộc sống.



