Như chúng ta đã biết mọi vật thể trong tự nhiên cũng như nhân tạo đều được cấu tạo từ chất này hay chất khác. Vì vậy, câu hỏi tiếp theo là những chất này đến từ đâu? Đây là câu hỏi đã được đặt ra hàng ngàn năm nay và được các nhà khoa học giải đáp bằng khái niệm ” nguyên tử “. Hãy cùng manta.edu.vn tìm hiểu chi tiết qua bài viết dưới đây nhé!
Lịch sử nghiên cứu về nguyên tử trong hóa học
Trên thực tế, khái niệm nguyên tử đã được đề cập từ hàng ngàn năm trước. Lịch sử nghiên cứu về nguyên tử được chia thành nhiều thời kỳ, bao gồm: Hy Lạp cổ đại, thế kỷ 18, lý thuyết nguyên tử ở thế kỷ 19 và thời của Giáo sư Vật lý Henri Becquerel và Marie Curie.
Lý thuyết nguyên tử có nguồn gốc từ tiếng Hy Lạp cổ đại Atomos (không thể chia cắt). Theo đó, vật chất bao gồm các hạt rời rạc. Thuyết nguyên tử là một trong nhiều cách giải thích về vật chất và không gian dựa trên dữ liệu thực nghiệm.
Một số mốc quan trọng của lý thuyết khoa học về nguyên tử:

-
1805: John Dalton là nhà hóa học, vật lý học và nhà khí tượng học nổi tiếng người Anh. Ông cũng là một trong những người tiên phong của lý thuyết nguyên tử hiện đại, sử dụng khái niệm nguyên tử để giải thích tại sao các nguyên tố luôn phản ứng theo những số tự nhiên nhỏ và có những chất khí có thể hòa tan. trong nước tốt hơn so với các khí khác.
“Mỗi nguyên tố hóa học chứa các nguyên tử cùng loại, duy nhất và các nguyên tử này kết hợp với nhau để tạo thành các hợp chất hóa học.” (Wikipedia.org)
Trong thuyết nguyên tử này không có thông tin về kích thước cụ thể của nguyên tử mà chỉ được xác nhận qua giác quan là “rất nhỏ”.
-
Năm 1827: Robert Brown – Nhà thực vật học nổi tiếng người Scotland đã dùng kính hiển vi để quan sát các hạt bụi nổi trên mặt nước. Lúc này, anh nhận ra rằng chúng di chuyển theo hình zíc zắc.
-
1865: Johann Josef Loschmidt – nhà khoa học người Áo có bước đột phá trong nghiên cứu về nguyên tử. Cụ thể, ông đã tìm ra kích thước của các phân tử trong không khí.
-
1905: Albert Einstein – Nhà vật lý vĩ đại người Đức đã phân tích thành công khối lượng và kích thước của nguyên tử và khẳng định thuyết nguyên tử của nhà hóa học kiêm vật lý John Dalton.
Khái niệm Nguyên tử là gì?
Trên thực tế, có hàng chục triệu chất khác nhau, nhưng chỉ có khoảng 100 loại nguyên tử. Nguyên tử được hình dung như một quả cầu rất nhỏ, đường kính chỉ khoảng 0,00000001 cm.
SGK Hóa học 8 (NXBGDVN) định nghĩa nguyên tử như sau:
“Nguyên tử là hạt vô cùng nhỏ và trung hòa về điện. Một nguyên tử bao gồm một hạt nhân tích điện dương và lớp vỏ được tạo thành từ một hoặc nhiều electron tích điện âm .
Electron ký hiệu là e có điện tích âm nhỏ nhất và được quy ước mang dấu âm (-).
Nguyên tử được cấu tạo từ những hạt nào?
Dựa vào định nghĩa nguyên tử là gì ở trên, chúng ta có thể thấy rõ nguyên tử được cấu tạo từ hai loại gồm hạt nhân mang điện tích dương và lớp vỏ được tạo thành từ một hay nhiều electron mang điện tích âm.
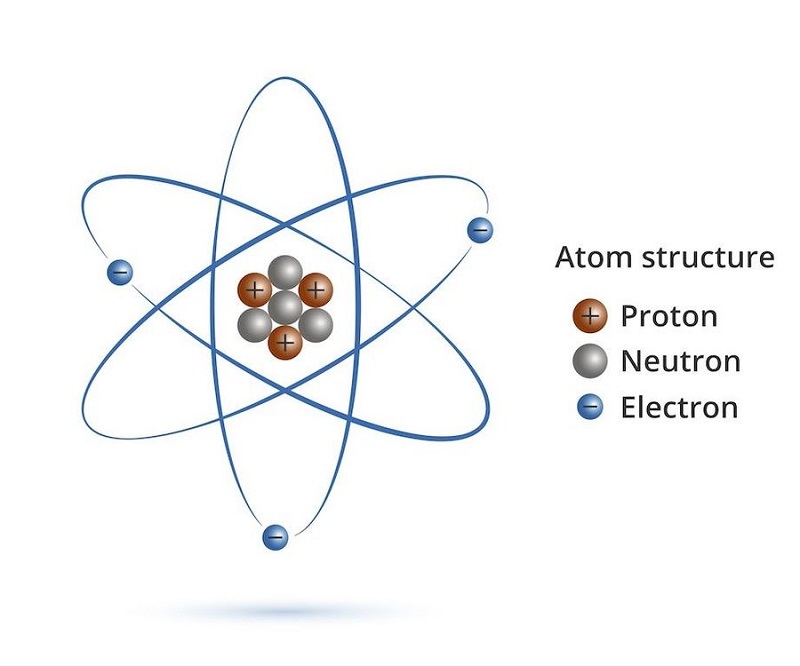
Một số khái niệm khác liên quan đến nguyên tử
Để hiểu bản chất của nguyên tử là gì, chúng ta cũng nên tìm hiểu một số khái niệm liên quan đến nguyên tử, bao gồm hạt nhân nguyên tử, lớp vỏ electron trong nguyên tử hay định nghĩa khối lượng nguyên tử.

Hạt nhân
Hạt nhân nguyên tử được tạo thành từ các proton và neutron , nằm ở trung tâm của nguyên tử. Proton được ký hiệu là p và có cùng điện tích với electron nhưng khác dấu (được biểu thị bằng dấu + dương). Nơtron không mang điện tích, kí hiệu n. Các nguyên tử cùng loại có cùng số proton trong hạt nhân.
Có nhiều proton trong một nguyên tử như có điện tử. Kết luận số p = số e . Trên thực tế, proton và neutron có cùng khối lượng, và electron có khối lượng rất nhỏ, chỉ bằng khoảng 0,0005 lần khối lượng của proton. Do đó, các nhà khoa học coi khối lượng của hạt nhân là khối lượng của nguyên tử .
Lớp electron trong nguyên tử
Trong nguyên tử, các electron luôn chuyển động rất nhanh xung quanh hạt nhân và sắp xếp thành từng lớp có số electron nhất định. Và nhờ có electron mà các nguyên tử có khả năng liên kết với nhau.
Số nguyên tử
Trong bảng tuần hoàn, mỗi phân tử có số nguyên tử riêng. Dựa vào số hiệu nguyên tử, chúng ta có thể phân biệt nguyên tố này với nguyên tố khác.
số nguyên tử là gì? Số nguyên tử là số proton được tìm thấy trong hạt nhân nguyên tử của nguyên tố hóa học đó. Trong trường hợp nguyên tử không mang điện tích, số lượng nguyên tử bằng số lượng electron.
khối nguyên tử
“Khối lượng nguyên tử là khối lượng của một nguyên tử tính bằng đơn vị cacbon. Mỗi nguyên tố có nguyên tử khối riêng biệt” (SGK Hóa học 8, NXB Giáo dục Việt Nam).
Do nguyên tử có khối lượng rất nhỏ, sử dụng không tiện nên các nhà khoa học đã quy ước lấy 1/12 khối lượng của nguyên tử cacbon làm đơn vị khối lượng cho nguyên tử (viết tắt là dc).
Phân biệt giữa nguyên tử và phân tử
Trong quá trình tìm hiểu về nguyên tử, rất nhiều bạn nhầm lẫn giữa nguyên tử và phân tử. Vậy làm thế nào để phân biệt hai khái niệm này? ài tập củng cố kiến thức bài nguyên tử
|
Đặc điểm so sánh |
Nguyên tử |
Phân tử |
|
Khái niệm |
Nguyên tử là hạt vô cùng nhỏ và trung hòa về điện. Nguyên tử gồm hạt nhân mang điện tích dương và vỏ tạo bởi một hay nhiều electron mang điện tích âm. |
Phân tử là hại đại diện cho chất, gồm một số nguyên tử liên kết với nhau và thể hiện đầy đủ tính chất hóa học của chất. |
|
Ví dụ |
Nguyên tử oxi, nguyên tử cacbon |
Oxy (O2), nước (H2O) |
|
Hình dạng |
Hình cầu |
Nhiều hình dáng |
|
Tính chất |
Không thể phân đôi nguyên tử |
Các nguyên tố trong phân tử có thể tách rời và kết hợp với nhau. |
|
Sự tồn tại |
Có thể tồn tại hoặc không tồn tại ở trạng thái tự do |
Tồn tại trong trạng thái tự do |
|
Tầm nhìn |
Không nhìn thấy bằng mắt thường |
Không thể nhìn thấy bằng mắt thường nhưng nếu có kính hiển vi vẫn có thể quan sát |
|
Khả năng phản ứng |
Phản ứng cao, có ngoại lệ nhất định |
Ít phản ứng |
|
Liên kết |
Liên kết hạt nhân |
Liên kết cộng hóa trị hoặc liên kết cộng ion |
Bài tập củng cố kiến thức bài học về nguyên tử
Sau khi nắm chắc lý thuyết, đừng quên làm các bài tập trong sách giáo khoa, sách bài tập hay sách bổ trợ để ghi nhớ kiến thức chắc chắn hơn. Dưới đây là một số bài tập được manta.edu.vn tổng hợp từ sách giáo khoa Hóa học 8 (NXB Giáo dục Việt Nam) có đáp án gợi ý cho các bạn tham khảo.

Bài 1: Ôn tập về khái niệm nguyên tử
“(1) là hạt cực nhỏ trung hòa về điện: từ tính (2) tạo ra mọi chất. Nguyên tử gồm (3) mang điện tích dương và vỏ làm bằng (4)”.
Câu trả lời gợi ý:
(1): Nguyên tử
(2): nguyên tử
(3) hạt nhân
(4) một hoặc nhiều electron tích điện âm
Bài 2: Bài tập ôn tập SGK Hóa học 8 trang 25
Đồng và sắt được làm từ nguyên tố nào? Nêu cách sắp xếp các nguyên tử trong nguyên tố kim loại.
Câu trả lời gợi ý:
Kim loại đồng được tạo thành từ nguyên tố Cu; kim loại sắt được tạo thành từ nguyên tố Fe;
Sự sắp xếp của các nguyên tử trong một nguyên tố kim loại: Chúng được sắp xếp gần nhau và theo một trật tự xác định.
Nguyên tử là một bài học quan trọng trong chương trình Hóa học THCS. Vì vậy, các em đừng quên ôn tập thật kỹ kiến thức cũng như làm bài tập đầy đủ để nắm vững kiến thức của bài học này nhé. manta.edu.vn chúc các bạn học tập thật tốt!



