Axit axetic (hay còn gọi là giấm ăn) là dung dịch thu được khi lên men rượu etylic loãng. Lượng tiêu thụ axit axetic trên toàn thế giới lên tới 6,5 triệu tấn mỗi năm. Tìm hiểu công thức, tính chất, ứng dụng và bài tập thực tế của chất quen thuộc này.
Định nghĩa axit axetic là gì?
Axit axetic là một hợp chất hữu cơ có tính axit khá mạnh . Hóa chất này đã được sản xuất từ rất lâu cũng như ứng dụng nhiều trong sản xuất thực phẩm, công nghiệp hay y học…
Công thức rút gọn: CH3COOH
Gồm nhóm -OH liên kết với nhóm C=O tạo thành nhóm -COOH, chính nhóm -COOH (Cacboxyl) làm cho phân tử có tính axit, tạo nên tính chất hóa học đặc trưng của axit axetic.
Nó cũng là một chất lỏng không màu và một hợp chất hữu cơ axit . Giấm có tối thiểu 4% axit axetic theo thể tích. Điều đó làm cho axit axetic trở thành thành phần chính trong giấm bên cạnh nước.
Ngoài tên gọi trên, sản phẩm này còn được biết đến với các tên gọi khác như: Ethanoic, Hydrogen Acetate (HAc), Axit Ethylic, Axit cacboxylic mêtan, giấm, axit axetic, Axit Ethanol…

-
Công thức hóa học: CH3CO2H
-
Khối lượng phân tử: 60
-
Cấu trúc phân tử:
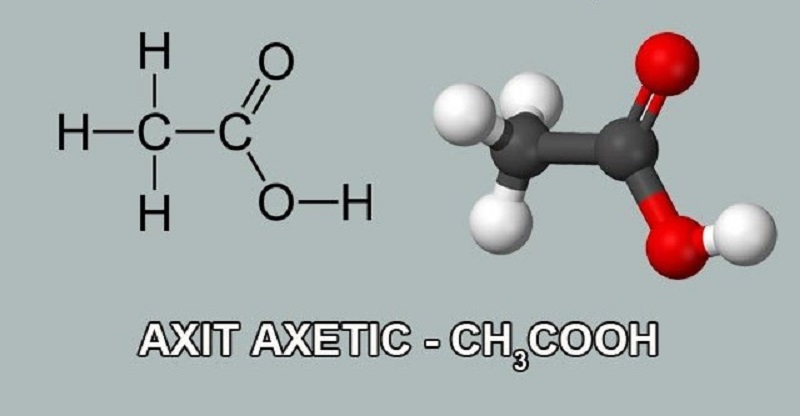
Tính chất vật lý của axit axetic là gì?
Các tính chất vật lý của axit axetic (CH3COOH) như sau:
-
Đây là một chất lỏng không màu. Khi bạn nếm nó, nó có vị chua. Chúng tan vô hạn trong nước.
-
Tỷ trọng axit axetic: 1,049 g/cm3 (l), 1,266 g/cm3 (s).
-
Nhiệt độ nóng chảy : 16,5 độ C.
-
Điểm sôi của axit axetic là: 118,2 độ C. Nhiệt độ sôi của chất này cao hơn rượu mặc dù chúng có cùng phân tử khối do có liên kết bền trong phân tử hiđro. Ngoài ra, do gốc OH của axit axetic phân cực hơn gốc ROH (ancol) nên khả năng tạo liên kết hiđro cũng lớn hơn gốc OH của ancol. Nhiệt độ sôi của các chất có cùng phân tử khối với axit axetic được sắp xếp như sau:
CH3COOH > CH3CH2OH > CH3-COO-CH3 > CH3-CHO > CH3CH2Cl > C2H6
-
Khi đun nóng, axit axetic có khả năng hòa tan một lượng nhỏ lưu huỳnh và phốt pho.
-
Phân tử axit axetic là phân tử phân cực nên ngoài khả năng tan tốt trong hợp chất phân cực như nước còn tan tốt trong hợp chất không phân cực như dầu mỏ, hexan, xenlulozơ và nhiều nguyên tố hóa học khác như: lưu huỳnh. và iốt.
Tính chất hóa học của axit axetic
Nguyên tử hydro trong nhóm cacboxyl có khả năng cho một proton H+ và làm cho axit axetic có tính axit. Điều này xác định tính chất hóa học của axit axetic.
Axit axetic là một axit yếu – có đầy đủ tính chất của một axit
Để chứng minh axit axetic là axit yếu người ta tiến hành thí nghiệm sau. Cho dung dịch axit axetic lần lượt vào các ống nghiệm chứa các chất sau: quỳ tím hóa xanh, dung dịch NAOH với phenolphtalein, CuO, Zn, Na2CO3.
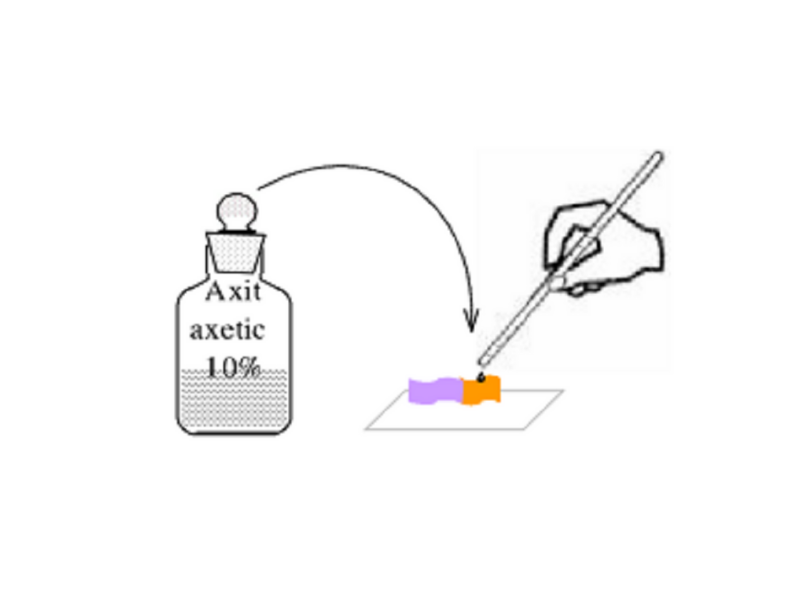
Hiện tượng của các thí nghiệm này là gì?
- Dung dịch axit axetic làm quỳ tím chuyển sang màu đỏ .
- Khi nhỏ dung dịch axit axetic vào ống nghiệm chứa Zn thì mẫu Zn tan dần, trong dung dịch có khí không màu thoát ra. phương trình:
Zn + 2CH3COOH→ (CH3COO)2Zn+ H2↑
- Khi nhỏ dung dịch axit axetic vào ống nghiệm chứa CuO thì bột CuO tan dần, dung dịch chuyển từ không màu sang màu xanh lam. phương trình:
CuO + 2CH3COOH→ (CH3COO)2Cu+ H2O
- Khi cho dung dịch axit axetic vào ống nghiệm chứa NaOH tác dụng với phenolphtalein thì màu hồng của dung dịch trong ống nghiệm biến mất. phương trình:
NaOH + CH3COOH → CH3COONa H2O
- Khi nhỏ dung dịch axit axetic vào ống nghiệm chứa Na2CO3 thì Na2CO3 tan dần, có khí không màu thoát ra khỏi dung dịch. phương trình:
Na2CO3+ 2CH3COOH → 2CH3COONa + CO2↑ + H2O
Từ các thí nghiệm trên, có thể rút ra kết luận về tính chất hoá học của axit axetic như sau:
- Axit axetic là một axit hữu cơ có tính chất của một axit . Tuy nhiên, đây là một axit yếu thuộc nhóm axit monoprotic.
- Axit axetic phản ứng với bazơ, cacbonat và bicacbonat. Khi cho các chất trên phản ứng với nhau, sản phẩm tạo ra sẽ là kim loại tương ứng axetat, nước và khí cacbonic. Phổ biến nhất là natri bicacbonat với giấm. phương trình:
NaHCO3 + CH3COOH → CH3COONa + CO2 + H2O
- Axit axetic phản ứng với kiềm để tạo ra nước và ethanoate kim loại. Phương trình: NaOH + CH3COOH → CH3COONa + H2O
- Axit axetic khi bị phân hủy ở nhiệt độ lớn hơn 440 độ C sẽ tạo thành cacbonic, metan hoặc etilen và nước.
- Axit axetic phản ứng với kim loại đứng trước H , giải phóng H2. Axit axetic có khả năng ăn mòn nhiều kim loại khác nhau tạo ra khí hiđro và muối axetat. Ví dụ, khi chúng phản ứng với nhôm, phương trình hóa học là:
Mg + 2CH3COOH → (CH3COO)2Mg + H2
- Nhôm thụ động với axit axetic vì khi phản ứng, axit này tạo ra một màng mỏng trên bề mặt nhôm oxit để ngăn chặn sự ăn mòn hóa học. Đó là lý do thùng nhôm thường được dùng để đựng axit axetic.
- Axit axetic phản ứng với muối của axit yếu hơn , ví dụ:
2CH3COOH + CaCO3 → (CH3COO)2 Ca + CO2 + H2O
Axit axetic tác dụng với rượu etylic
Để biết axit axetic phản ứng với rượu etylic như thế nào, người ta làm thí nghiệm sau. Cho ancol etylic, axit axetic vào ống nghiệm A, thêm một ít axit sunfuric đặc làm xúc tác. Đun sôi hỗn hợp một lúc thì dừng lại. Thêm một ít nước vào phần hơi nước ngưng tụ trong ống nghiệm B, lắc nhẹ rồi quan sát.
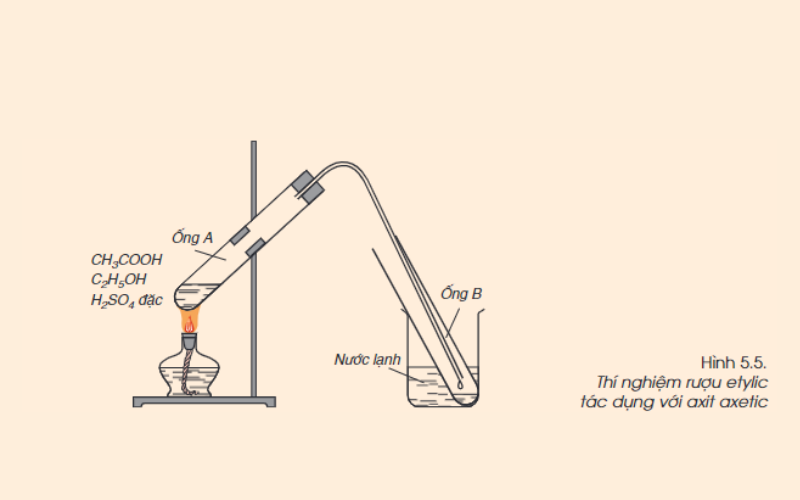
Một lúc sau ta quan sát thấy hiện tượng: Trong ống nghiệm B có chất lỏng không màu, mùi thơm, không tan trong nước, nổi trên mặt nước.
Do đó, rượu etylic phản ứng với axit axetic tạo ra etyl axetat. Đây là chất lỏng, có mùi thơm, ít tan trong nước, được dùng làm dung môi trong công nghiệp.
Phản ứng trên xảy ra theo phương trình hóa học:
C2H5OH + CH3COOH CH3COOC2H5 + H2O ( H2S04 đặc, nhiệt độ)
Cách điều chế axit axetic
Hiện nay có nhiều phương pháp điều chế axit axetic. Chi tiết:

Điều chế axit axetic từ rượu etylic
Để sản xuất giấm, người ta thường dùng phương pháp lên men từ dung dịch rượu etylic loãng theo phương trình:
CH3CH2OH + O2 → CH3COOH + 2H2O (xúc tác: Men giấm)
Chú ý: Các hợp chất hữu cơ trong phân tử có chứa nhóm -COOH, có công thức CnH2n+1 COOH được gọi là axit cacboxylic no đơn chức và có tính chất tương tự axit axetic.
oxy hóa butan
Trong công nghiệp, axit axetic thương mại được sản xuất từ butan C4H10 với sự có mặt của chất xúc tác và nhiệt độ, diễn ra theo phương trình:
2C4H10 + 5O2 → 4CH3COOH+ 2H2O (xúc tác, nhiệt độ)
Axit butan axetic
Ứng dụng quan trọng của axit axetic
Nhu cầu về axit axetic trên toàn thế giới là khoảng 6,5 triệu tấn mỗi năm. Sau đây là những ứng dụng quan trọng và phổ biến nhất của axit axetic trong đời sống.
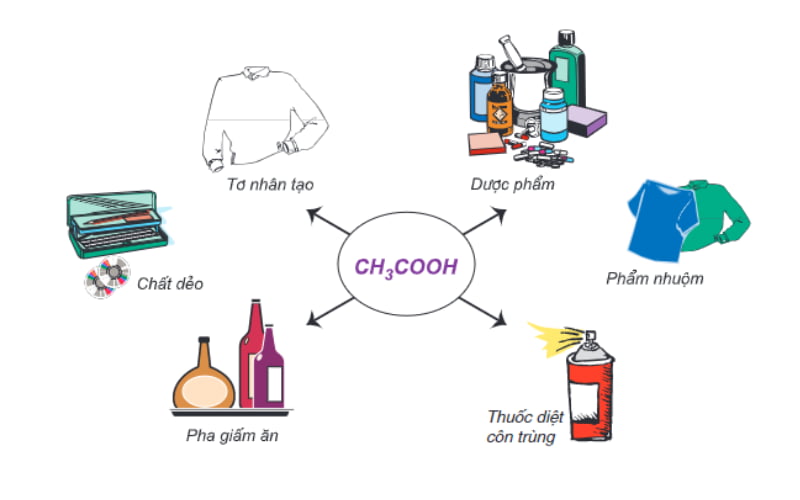
Ứng dụng của axit axetic trong công nghiệp
-
Khoảng 40% đến 45% sản lượng axit axetic trên thế giới được sử dụng để sản xuất monome vinyl axetat, chất kết dính và chất sơn .
-
Dùng làm dung môi hoặc dùng để tạo độ chua nhẹ.
-
Giấm là dung dịch axit axetic 5-7%. Giấm ăn được dùng trong công nghiệp thực phẩm để chế biến đồ hộp, rau, củ, quả, gia vị,….
-
Sử dụng như một chất tẩy cặn vôi từ vòi và ấm đun nước.
-
Axit axetic được dùng trong dệt nhuộm, cao su, hóa chất xi mạ.
Ứng dụng của axit axetic trong y học
-
Axit axetic có đặc tính kháng khuẩn hiệu quả và được sử dụng làm chất khử trùng (pha loãng 1%). Nó có thể được sử dụng như một phương pháp thay thế để ngăn ngừa nhiễm trùng và tiêu diệt vi khuẩn.
-
Axit axetic được bào chế thành thuốc chống tiểu đường .
Ứng dụng của axit axetic đối với con người (hàm lượng 4-8%)
-
Axit axetic ức chế quá trình thủy phân disacarit thành đường đơn và giúp giảm tăng đường huyết sau ăn , góp phần giảm cân.
-
Giấm chứa axit axetic giúp ngăn chặn quá trình tích tụ mỡ trong cơ thể và gan, giảm lượng calo đưa vào cơ thể mỗi ngày, từ đó giúp giảm béo.
-
Giấm táo là một loại thuốc chống lão hóa hiệu quả.
-
Axit axetic là một axit hữu cơ có tính chất của một axit cụ thể, phản ứng với kim loại để tạo ra muối trung hòa. Điều này mang lại cho axit axetic khả năng hòa tan sỏi thận.
Axit axetic có độc không? Nó ảnh hưởng như thế nào đến sức khỏe con người?
Các chuyên gia hóa học cho biết, bản thân axit axetic không độc đối với cơ thể con người nhưng nếu sử dụng với liều lượng lớn có thể dẫn đến tử vong. (Nguồn: báo Thanh Niên)

-
Ảnh hưởng đến hệ hô hấp: Hít phải một lượng lớn axit axetic gây kích ứng mũi, họng và phổi, gây tổn thương nghiêm trọng cho niêm mạc của các cơ quan mũi và sau đó là khó thở.
-
Kích ứng da: Khi tiếp xúc với da sẽ gây kích ứng như đau, mẩn đỏ và nổi mụn nước, nặng hơn là bỏng sau vài phút tiếp xúc.
-
Đe dọa tính mạng: Nuốt phải axit axetic có thể gây xói mòn nghiêm trọng miệng và đường tiêu hóa, dẫn đến nôn mửa, tiêu chảy, suy tuần hoàn, suy thận và tử vong.
Theo bác sĩ Nguyễn Thị Huỳnh Mai, Chi cục trưởng Chi cục An toàn vệ sinh thực phẩm TP.HCM, giấm là chất lỏng có vị chua, được hình thành từ quá trình lên men, có nhiều lợi ích cho sức khỏe. mạnh. Axit axetic chỉ chiếm một tỷ lệ nhỏ trong giấm (từ 3 đến 5%), khiến giấm có vị chua. Nhưng nếu sản xuất giấm từ nước pha axit axetic công nghiệp sẽ gây hại cho sức khỏe người dùng. (Nguồn: Báo Thanh Niên)
Giấm mang nhiều chất dinh dưỡng bao gồm vitamin, axit amin và axit hữu cơ, mang lại nhiều lợi ích cho sức khỏe. Tuy nhiên, để đảm bảo an toàn khi sử dụng, người tiêu dùng cần cẩn trọng trong việc lựa chọn giấm. An toàn nhất, người tiêu dùng nên mua giấm ở những cơ sở uy tín , ngoài ra, có thể tự lên men, làm giấm tại nhà để sử dụng.
Bài tập SGK axit axetic có lời giải
Từ những kiến thức về axit axetic ở trên, các em sẽ vận dụng những kiến thức đó để giải một số bài tập cơ bản trong SGK hóa học 9 sau đây.

Giải bài 1 trang 143 SGK Hóa học 9
Điền vào chỗ trống những từ thích hợp:
a) Axit axetic là chất … không màu, không vị… tan… trong nước.
b) Axit axetic là nguyên liệu để điều chế…
c) Giấm là dung dịch … từ 2 đến 5%
d) Bằng … butan có xúc tác thích hợp người ta thu được…
Câu trả lời gợi ý:
a) Axit axetic là chất lỏng không màu, có vị chua, tan vô hạn trong nước.
b) Axit axetic là nguyên liệu để điều chế dược phẩm, thuốc nhuộm, chất dẻo, tơ nhân tạo.
c) Giấm là dung dịch axit axetic có nồng độ từ 2 đến 5%.
d) Oxi hóa butan với xúc tác thích hợp thu được axit axetic.
Giải bài 5 SGK Hóa 9 trang 143
Axit axetic có thể phản ứng với chất nào sau đây: ZnO, Na2SO4, KOH, Na2CO3, Cu, Fe? Viết các phương trình hóa học xảy ra (nếu có).
Câu trả lời gợi ý:
Các chất có thể phản ứng với axit axetic là ZnO, KOH, Na2CO3, Fe.
2CH3COOH + ZnO → (CH3COO)2Zn + H2O.
CH3COOH + KOH → CH3COOK + H2O.
2CH3COOH + Na2CO3 → 2CH3COONa + CO2 + H2O.
2CH3COOH + Fe → (CH3COO)2Fe + H2.
Giải bài 6 trang 143 SGK Hóa học 9
Viết phương trình hóa học điều chế axit axetic từ:
a) Natri axetic và axit sunfuric.
b) Rượu etylic.
Câu trả lời gợi ý:
Phương trình phản ứng điều chế axit axetic:
a) Từ natri axetic và axit sunfuric:
2CH3COONa + H2SO4 → 2CH3COOH + Na2SO4
b) Từ rượu etylic:
C2H5OH + O2 → CH3COOH + H2O.
Giải bài 7 SGK Hóa 9 trang 143
Cho 60g CH3COOH phản ứng với 100g CH3CH2OH thu được 55g CH3COOCH2CH3
a) Viết phương trình hóa học xảy ra và gọi tên phản ứng.
b) Tính hiệu suất của phản ứng trên
Câu trả lời gợi ý:
n(CH3COOH) = 60/60 = 1 mol
n(C2H5OH) = 100/46 = 2,17mol
a) Phương trình phản ứng:
CH3COOH + C2H5OH → CH3COOC2H5 + H2O
Phản ứng này được gọi là phản ứng este hóa.
b) Hiệu suất của phản ứng:
Theo phương trình phản ứng trên và dữ liệu bài toán đã cho, số mol ancol dự kiến, từ đó tính hiệu suất phản ứng theo CH3COOH.
Về lý thuyết 1 mol CH3COOH (60g) tạo ra 1 mol CH3COOC2H5 (88g) nhưng thực tế chỉ thu được 55g.
Vậy hiệu suất của phản ứng là: H% = 55/88 x 100% = 62,5%
Một số bài tập về axit axetic cho học sinh tự luyện
Câu 1: Ứng dụng nào sau đây không phải của axit axetic?
A. Pha giấm
B. Sản xuất dược phẩm, thuốc nhuộm, thuốc diệt côn trùng
C. Sản xuất rượu
D. Sản xuất plastic, tơ nhân tạo
Câu 2: Để phân biệt C2H5OH và CH3COOH, dùng hóa chất nào sau đây đúng?
A. Na B. Dung dịch AgNO3 C. CaCO3 D. NaCl . giải pháp
Câu 3: Cho các phản ứng sau ở điều kiện thích hợp:
1, Lên men giấm rượu etylic
2, Oxi hóa không hoàn toàn anđehit axetic
3, Oxi hóa không hoàn toàn Butan
4, Cho metanol phản ứng với cacbon oxit. Trong số các phản ứng trên, số phản ứng tạo ra axit axetic
A. 1 B. 2 C. 3 D. 4
Câu 4: Yếu tố nào không làm tăng hiệu suất phản ứng este hóa giữa axit axetic và etanol?
A. Dùng H2SO4 đặc làm xúc tác B. Chưng cất este tạo ra
C. Tăng nồng độ axit hoặc rượu D. Lấy số mol rượu và axit bằng nhau
Câu 5: Vì sao nhiệt độ sôi của axit thường cao hơn ancol tương ứng?
A. Vì ancol không có liên kết hiđro nên axit có liên kết hiđro
B. Vì liên kết hiđro của axit mạnh hơn của ancol
C. Vì phân tử khối của axit lớn hơn
D. Vì axit có 2 nguyên tử oxi
Câu 6: Giấm ăn là dung dịch axit axetic có nồng độ là
A. 2% đến 5% B. 6% đến 10% C. 11% đến 14% D. 15% đến 18%
Câu 7: Chia a gam axit axetic thành 2 phần bằng nhau:
-Phần 1: trung hòa vừa đủ bởi 0,5 lít dd 0,4M. dung dịch NaOH
-Phần 2: thực hiện phản ứng este hóa với ancol etylic thu được m gam este (giả sử hiệu suất phản ứng là 100%). Vậy m có giá trị là:
A. 16,7 gam B. 17,6 gam C. 16,8 gam D. 18,6 gam
Câu 8: Để tách riêng các chất với nhau ra khỏi hỗn hợp axit axetic và ancol etylic, có thể làm cách nào sau đây?
A. Dùng CaCO3, chưng cất rồi phản ứng với H2SO4
B. Dùng CaCCl2, chưng cất rồi phản ứng với H2SO4
C. Dùng Na2O rồi tác dụng với H2SO4
D. Dùng NaOH rồi phản ứng với H2SO4
Câu 9: Cho một axit có nồng độ x% tác dụng vừa đủ với dung dịch NaOH có nồng độ 10% thu được dung dịch muối có nồng độ 10,25%. Vậy x có giá trị là:
A. 20% B. 16% C. 17% D. 15%
Câu 10: Phương pháp được coi là hiện đại để điều chế axit axetic là:
A. Tổng hợp từ CH3OH và CO B. Phương pháp oxi hóa CH3CHO
C. Phương pháp lên men giấm từ rượu etylic D. Điều chế từ muối axetat
Câu 11: Dãy chất phản ứng được với axit axetic là
A. ZnO, Cu, Na2CO3, KOH B. ZnO, Fe, Na2CO3, Ag
C. SO2, Na2CO3, Fe, KOH D. ZnO, Na2CO3, Fe, KOH
Câu 12: Khi đun nóng axit axetic với ancol etylic có axit sunfuric làm xúc tác thu được một chất lỏng không màu, mùi thơm, không tan trong nước, nổi trên mặt nước. Sản phẩm đó là
A. đimetyl ete B. etyl axetat C. ancol etylic D. metan
Câu 13: So sánh nhiệt độ sôi của các chất: Axit axetic, axeton, propan, etanol
A. CH3COOH > CH3CH2CH3 > CH3COCH3 > C2H5OH
B. C2H5OH>CH3COOH>CH3CH2CH3> CH3COCH3
C. CH3COOH>C2H5OH>CH3COCH3>CH3CH2CH3
D. C2H5OH>CH3COCH3>CH3COOH>CH3CH2CH3
Câu 14: So sánh tính axit của các chất sau (theo thứ tự tăng dần: CH3CHClCH2COOH (1); CH2ClCH2CH2COOH (2); CH3CH2CHClCOOH (3)CH3CH2CH2COOH (4)
A. 1< 3< 2< 4 B. 2< 1< 3< 4 C. 4< 3< 2< 1 D. 4< 2< 1< 3
Câu 15 : Cho 1 gam axit axetic vào ống nghiệm thứ nhất và 1 gam axit fomic vào ống nghiệm thứ hai, sau đó cho vào cả hai ống nghiệm một lượng dư bột CaCO3. Khi phản ứng xảy ra hoàn toàn, thể tích khí CO2 thu được ở cùng nhiệt độ và áp suất là:
A. Hai ống bằng nhau B. Ống 1 nhiều hơn ống 2
C. Ống 2 nhiều hơn ống 1 D. Cả hai ống nhiều hơn 22,4 lít (đv)
Câu 16: Chọn phát biểu sai trong các phát biểu sau?
A. Axit axetic là chất lỏng, không màu, vị chua, tan vô hạn trong nước.
B. Axit axetic là nguyên liệu để điều chế dược phẩm, thuốc nhuộm, chất dẻo, tơ nhân tạo.
C. Giấm ăn là dung dịch axit axetic có nồng độ từ 2 đến 5%.
D. Oxi hóa etan với xúc tác thích hợp thu được axit axetic
Câu 17: Cho hỗn hợp axit axetic và một axit (X) thuộc dãy đồng đẳng của axit axetic. Để trung hòa hoàn toàn hỗn hợp này cần 300ml dung dịch Grate 0,2M. Làm bay hơi dung dịch sau phản ứng thu được 5,48 gam muối khan. Biết nCH3COOH : nX= 1 : 2. Công thức phân tử của X là:
A. HCOOH B. C2H5COOH C. CH3COOH D. C3H7COOH
Câu 18: Cho dung dịch axit axetic có nồng độ a% tác dụng vừa đủ với dung dịch NaOH có nồng độ 10%, thu được dung dịch muối có nồng độ 10,25%. Giá trị của a là gì:
A. 15% B. 20% C. 25% D. 30%
Câu 19: Cho 250 gam axit axetic phản ứng với 161 gam ancol etylic có H2SO4 đặc làm xúc tác. Khi phản ứng xảy ra hoàn toàn, 60% axit được chuyển thành este. Khối lượng este thu được khi kết thúc phản ứng là:
A. 220 gam B. 230 gam C. 235 gam D. 240 gam
Câu 20: Cho 20,5 gam hỗn hợp gồm ancol etylic và axit axetic phản ứng với kali dư thu được 4,48 lít H2 (đkc). Nếu cho hỗn hợp tham gia phản ứng este hóa thì khối lượng este thu được là bao nhiêu? Biết H= 100%
A. 10 gam B. 12 gam C. 13,2 gam D. 14,2 gam
Bài viết trên đã cung cấp đầy đủ thông tin về công thức, tính chất, ứng dụng và một số bài tập thực hành của axit axetic – một chất vô cùng phổ biến xung quanh chúng ta. Theo dõi chuyên mục Kiến thức cơ bản của Manta.edu.vn để biết thêm nhiều kiến thức bổ ích xoay quanh các môn Hóa, Toán, Lý…



